欧洲肌肉减少症工作组”提出了肌肉减少症的定义:一种综合征,表现为低肌肉力量,骨骼肌质量和数量下降,躯体活动能力下降,导致残疾、低生活质量及死亡等不良后果。
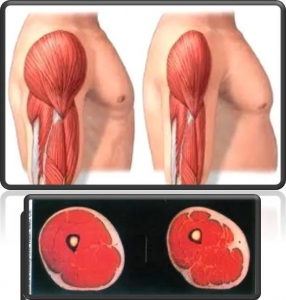
相比单纯因饥饿而导致的营养不良,发生了任何程度营养不良的肿瘤患者,不仅出现体质量(体重)的丢失 ,更有瘦肉群、脂肪群和体细胞群的明显减少。文献报道,肌肉减少症在肿瘤患者的发病率约21%~71%,不同肿瘤类型的发病率不尽相同。即使在同一肿瘤类型中,疾病所处不同阶段肌肉减少症的发病率也不同。肿瘤患者肌肉减少,目前认为,应归咎于患者体内促炎症因子产生过多和各种不良症状引起的摄食下降等为主要原因,导致患者机体能量营养素代谢状态的失衡,造成骨骼肌蛋白质分解加速和蛋白质合成不足。

在肿瘤内科,由于肿瘤相关肌肉减少症增加抗肿瘤药物治疗的不良反应发生率和严重程度、降低患者生活质量、甚至增加病死率 。因此,做好肿瘤患者的营养状态评估,及时发现肿瘤相关性肌肉减少症并加以干预非常重要。研究显示,单纯肌肉质量的提高并不能改善患者的活动能力,且低肌肉力量是肿瘤患者病死率的独立危险因素。结合了肌力和肌肉功能,对肿瘤患者进行综合评估后,所做出的肌肉减少症诊断,更能较全面和准确地评估其对肿瘤患者的预后的影响,及与化疗药物之间相关性的分析。
近十多年以来临床越来越意识到,肌肉减少症诊断必须综合评估肌肉质量及肌肉功能。其主要评估指标包括肌肉质量、肌肉力量及肌肉功能等。在肿瘤患者中,肌肉减少症可通过双能X 线吸收计量法(DEXA) 计算患者的四肢瘦软组织指标(ALST) 来进行诊断。男性低于7.26kg/m2,女性低于 5.45kg/ m2 。
肿瘤相关性肌肉减少症的发病机制相对复杂。尚无标准的治疗方案, 实施综合治疗主要方法就是通过营养支持和代谢调节增加蛋白质和能量摄入,并阻止肌肉的进一步减少。对肿瘤患者实施的营养代谢治疗,至少应包括营养补充、代谢调理、抗肿瘤治疗、梳理胃肠功能、减少耗能症状等五个方面。
营养补充可遵循中国抗癌协会肿瘤营养与支持治疗专业委员会的“营养不良五阶梯治疗原则”进行。能量需求多介于25~30kcal/(kg·d) 之间。对于卧床患者则可按照20~25kcal/(kg·d) 来估算总能量需求。蛋白质的补充应达到1~1.5g/(kg·d),同时合并急慢性肾功能不全的患者,应控制在1~1.2g/(kg·d),避免严重的负氮平衡。乳清蛋白是优质的动物蛋白质,消化率和利用率高,含有大量对肌肉蛋白平衡有益处的支链氨基酸,氨基酸组成与人体必需氨基酸需要量组成相似,具有促进肌肉蛋白质合成、防治肌肉减少的作用,同时还建议增加亮氨酸的摄入;代谢调理治疗就是应用一些具有药理学功效的营养素、生物激素或化学药物,对肿瘤患者实施抑制分解代谢和促合成代谢的调节治疗。

运动干预是十分重要的代谢调理治疗手段。2010年肌肉减少症预防与处理专家共识提出,运动(抗阻力及有氧运动均可)结合足量的蛋白质、能量摄入是防治肌肉减少症的关键措施。中等强度的运动,对于不同阶段的肿瘤患者均是安全的,可改善患者的有氧运动能力、肌肉力量、生活质量以及心理健康状况;而抗肿瘤治疗可以通过减少肿瘤负荷,来从根本上改善治疗患者的能量-营养素异常代谢状态。分为两个治疗阶段,第一阶段,联合营养治疗,适度减少肿瘤负荷,完成对营养不良状态的逆转。第二阶段,“标准方案”抗肿瘤治疗;至于发热、剧痛等症状可消耗大量的热量,胃肠功能紊乱、以及其它阻止患者食物摄取的症状诸如腹泻、厌食等,均应予以同步缓解甚至消除。